一篇读懂:锂矿百科|地采选冶、回收、供应链
谁是浩特?请参考下图

矿石提锂:含锂矿石主要包括锂辉石、锂磷铝石、锂云母、铁锂云母、透锂长石等。其中锂辉石是矿石提锂的重要来源之一,化学式为LiAL(AiO3)2,氧化锂的含量可达6%~9%,属单斜晶系,一般呈柱状、棒状产出,有时也呈板状或粒状。常与锂云母、绿柱石、铌钽铁矿、电气石、白云母等共生。
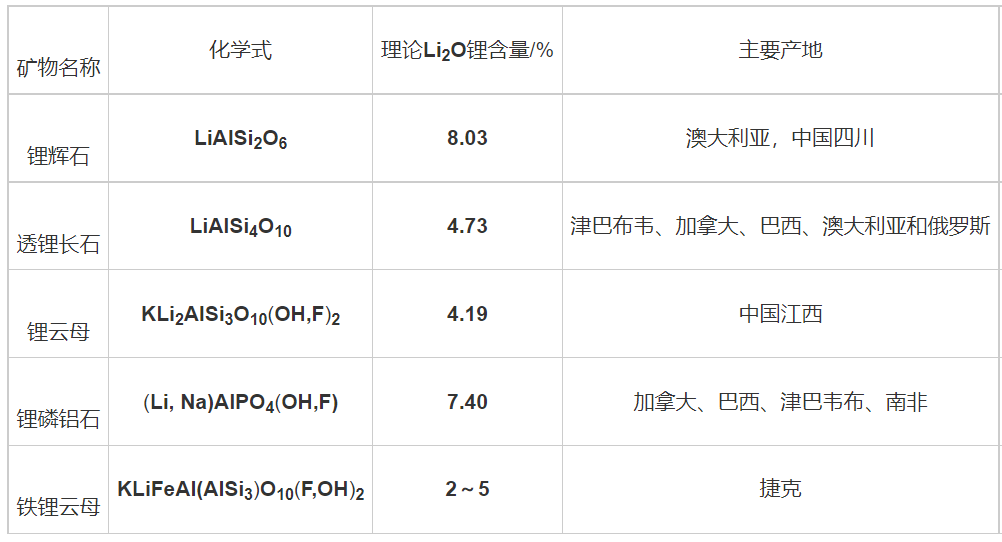
锂辉石是最重要且储量最大的锂矿石资源之一,是目前矿石提锂工艺的主要来源。全球锂辉石资源主要分布在澳大利亚、加拿大、和中国等地。澳大利亚西部的格林布什锂辉石矿床是全球最大的锂辉石矿床之一,折合碳酸锂储量为724万t。加拿大的锂辉石矿床均为中型矿床,折合碳酸锂储量均在160万t左右。

图锂辉石

图锂云母
盐湖提锂方法:
工艺路径 |
商业化盐湖 |
工艺优势 |
工艺劣势 |
盐田沉淀法 |
Atacama(SQM、ALB); SilverPeak;Olaroz; 西藏扎布耶 |
工艺成熟可靠;充分利用太阳能、盐湖的高蒸发率,生产成本低[27];方便生产钾等副产品 |
需建设大规模的盐田;只适合低MLR盐湖;受天气影响大,生产周期长;夹带损失严重,回收率低[16] |
吸附法 |
HombreMuerto(Livent)、 青海察尔汗、青海大柴旦、青海一里坪(五矿盐湖) |
较少的依赖盐田晒卤;生产成本低,效率高;契合当下DLE(Directlithiumextraction)技术的发展 |
淡水消耗大,综合利用钾肥需要额外投资;无机吸附剂的流动性差,循环性差,溶损严重 |
膜法 |
一里坪(五矿盐湖)、西台吉乃尔(中信国安)、西台吉乃尔(恒信融)、扎布耶(西藏矿业) |
反渗透膜可进行锂溶液的浓缩;纳滤膜可以实现一二价离子的分离(如镁离子和锂离子的分离);绿色环保 |
膜污染/膜堵塞,膜的回收率较低;膜通量与选择性难平衡 |
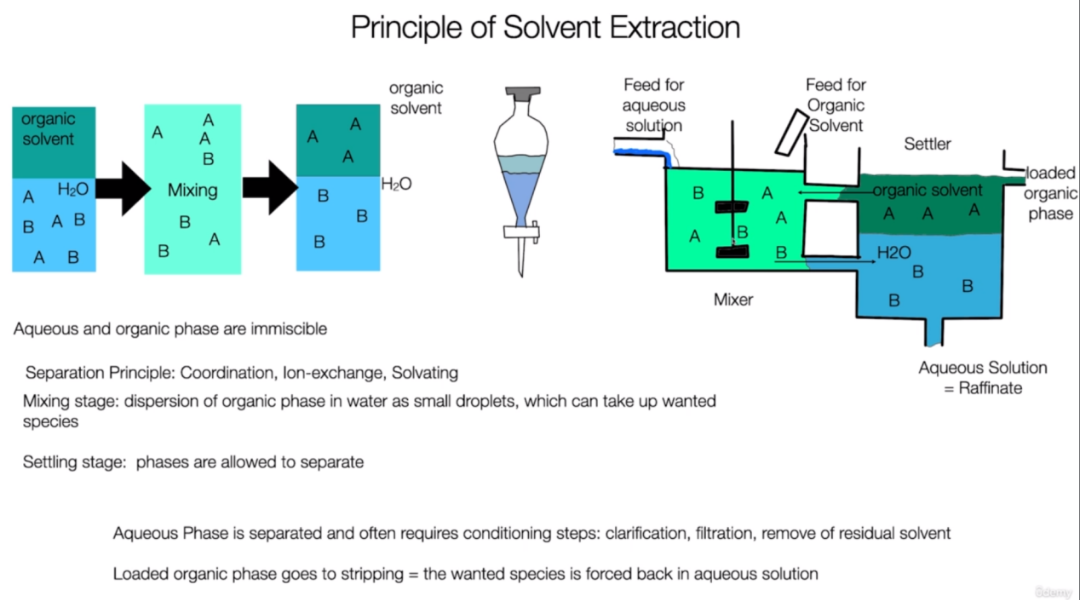
萃取法 |
青海大柴旦盐湖 |
分离效率高,回收率较高,可在常温常压下进行 |
萃取剂价格较昂贵;萃取过程在高酸性条件下进行,可能导致设备腐蚀,有机溶剂的环保压力大 |
电化学脱嵌法 |
西藏捌仟错,中南锂业专利 |
过程清洁、收率高、可原卤提锂、生产低且对卤水适应性强 |
盐湖卤水矿化度高、黏度大,会导致实际提锂速率较低 |
离子精馏法 |
暂无,中国科学技术大学研发,膜法延伸,已申请专利,实验室阶段 |
分离效率提升、对盐湖类型适应性强、对不同元素精细筛分 |
未明确 |
第一块锂矿石,透锂长石(LiAlSi4O10)是由巴西人在名为Utö的瑞典小岛上发现的,于18世纪90年代。当把它扔到火里时会发出浓烈的深红色火焰,斯德哥尔摩的JohanAugustArfvedson分析了它并推断它含有以前未知的金属,他把它称作lithium(锂)。他意识到这是一种新的碱金属元素。然而,不同于钠的是,他没能用电解法分离它。1821年WilliamBrande电解出了微量的锂,但这不足以做实验用。直到1855年德国化学家Robert Bunsen和英国化学家Augustus Matthiessen电解氯化锂才获得了大块的锂。
锂的英文为Lithium,来源于希腊文lithos,意为“石头”。Lithos的第一个音节发音“里”。因为是金属,在左方加上部首“钅”。锂在地壳中的含量比钾和钠少得多,它的化合物不多见,是它比钾和钠发现的晚的必然因素。锂发现的第二年,得到法国化学家伏克兰重新分析肯定。
NamelyPetalite(透锂长石):是长石类的矿物,具有单斜晶系,晶体结构为单斜晶系型。主要成分为硅酸钠钙锂,其中硅酸锂含量小于50%.具有良好的热稳定性和耐腐蚀性,可以用于制作耐酸碱性制品,如低膨胀、高耐热的陶瓷产品。
Spodumen(锂辉石):锂辉石是硅酸盐类的矿物,具有层状结构,组成单元为八面体,晶体结构为层状型。主要成分为硅酸锂,其中硅酸锂含量大于50%。
1818年,汉弗莱·戴维和布兰德用伏打堆电解氧化锂,制备了非常少量的金属锂。
伏打堆(Voltaicpile)是一种早期的电池装置,由意大利科学家亚历山大·伏打(AlessandroVolta)于不久后的1800年发明。伏打堆是由一系列交替堆叠的金属片和电解质湿纸片(通常浸泡在盐水中)组成的。每一对金属片之间都放置了电解质湿纸片,并通过将金属片和湿纸片交替堆叠,形成了一种电池电路。当两种不同的金属片接触电解质时,会产生电化学反应,从而产生电流。
在相当长的一段时间内,关于锂及其化合物并没有太多的兴趣。人们知道锂可以用于制药和玻璃制造,但那也就是它的用途。但在第一次世界大战后,锂开始再次引起人们的兴趣。它被用于一种基于铅的合金,该合金用于铁路轴承,这种特殊合金被称为“铁路合金”("bahnmetall"),这是一个德国词,意为“火车金属”。它含有0.04%的锂。这实际上是为什么现在需要大规模工业生产锂,特别是以碳酸锂和锂金属的形式。生产是使用含锂的矿物锡云母(zinwaldite)进行的,可以生产数吨的量。
由于现在碳酸锂容易获得,陶瓷工业也开始使用它。在第二次世界大战期间,锂的使用增加了,其中一个例子是锂氢化物(LithiumHydride)。在接下来的70年里,锂的使用越来越广泛,例如,基于锂的肥皂,它被用作多用途润滑剂和汽车工业或工业的润滑脂。此外,核工业也需要锂,在这种情况下,它们使用6Li来制备氚。如今,锂的最大消耗领域包括玻璃工业、陶瓷工业、铝生产、聚合物合成,尤其是弹性体,以及电池领域。
锂是周期表上的第三个元素,位于氢和氦之后,它拥有三个质子、三个中子和三个电子。它属于碱金属家族,与钠、钾、铷等元素类似,这意味着它只有一个价电子。地壳中的锂含量约为0.006%。

锂(Li)相对于碱金属族中的其他金属来说,它的反应性较低。碱金属族中的其他元素如钠(Na)、钾(K)、铷(Rb)和铯(Cs)通常比锂更活泼,更容易与空气中的氧气和水反应。锂因其独特的性能和相对稳定性,在多种应用场景中成为优选的金属。相较于其他碱金属,锂不易自燃或爆炸,更具安全性。因此,锂在电池制造、合金制备和其他工业应用中得到广泛的应用。

 新鲜的锂的表面为银色有光泽感的,在干燥的空气中能存留几天。在干燥的空气中锂的表面会生成非常薄的碳酸锂层(肉眼几乎不可见)。在潮湿的空气中,几秒内表面便会形成灰色的覆盖(Li2O、LiOHandLiN3)
新鲜的锂的表面为银色有光泽感的,在干燥的空气中能存留几天。在干燥的空气中锂的表面会生成非常薄的碳酸锂层(肉眼几乎不可见)。在潮湿的空气中,几秒内表面便会形成灰色的覆盖(Li2O、LiOHandLiN3)
保存锂:氩气或氮气,或在惰性矿物油中。锂遇水会释放氢气,氢气极易被点燃,爆炸。常见的灭火器:沙子,混凝土类的硅酸盐类,二氧化碳都会与其发生反应,不能用来灭火!!只有特殊的,石灰石或氯化钠的灭火器粉才行。细磨过的锂粉能在空气中自燃和爆炸。
锂是在室温下密度最小的固体。它的熔点为180度,在20℃时的密度为0.543g/cm3。锂的电离能较低,仅为5.37eV,其电极电位为-3.024V,使其成为最易释放电子的元素。因此,可以将锂与最负元素氟结合,以在理论上创建具有最佳性能的电池。
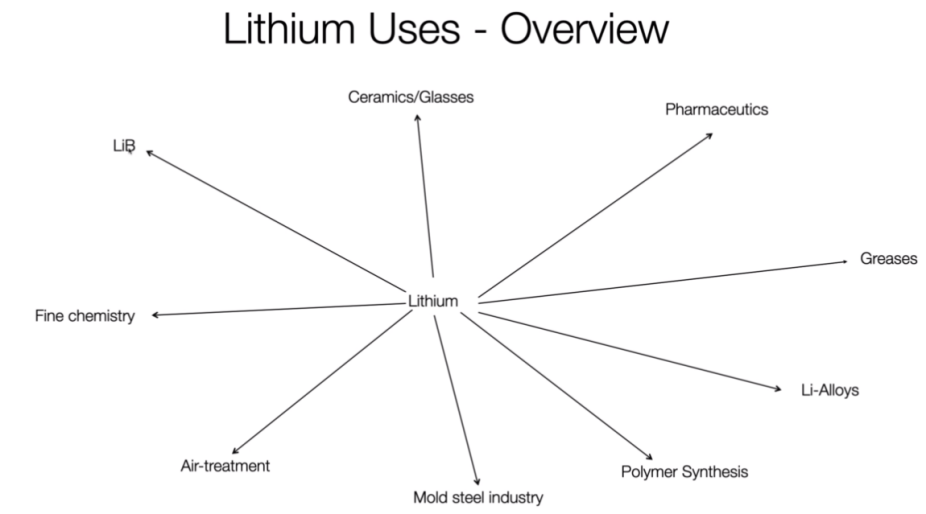
在制药行业,锂被用于制造药剂,如油脂和润滑剂等。
在空气处理领域,锂被用于制造特种气体,如用于电子工业的高纯度氮气和用于医疗领域的特殊气体。
锂可以在阴极材料中找到,所以是电池的正极部分。主要有钴酸锂(LCO)、锰酸锂(LMO)、磷酸铁锂(LFP)、三元材料(镍钴锰酸锂(NCM/NMC)和镍钴铝酸锂(NCA))等。除了用作电池的正极部分外,锂也可以用于锂离子电池的电解质,如六氟磷酸锂。
未来趋势:固态电解质取代液体电解质已有学者正在研究电导率超高的锂导电固态电解质。
陶瓷和玻璃也是使用锂的两个行业。陶瓷中加入少量锂辉石可降低烧结温度,缩短烧结时间。增强陶瓷的耐热、耐酸、耐碱、耐磨以及耐热急变性能。锂精矿或锂化物在制造玻璃时有较大的助熔作用,添加到玻璃配料中能够降低玻璃熔化时的温度和熔体的粘度,简化生产流程,降低能耗,增加产量。
65%的润滑剂中都含有一定量的锂,锂基润滑脂与钾、钠、钙基类的润滑脂相比,具有抗氧、耐压、润滑性能好的优点,锂使润滑剂变的稳定,在高温下不易分解,低温下不易凝固。含锂润滑剂中约含2%的锂。
铸钢行业。常添加助熔剂,使钢更容易熔化。这种助熔剂可以含有,例如,5%的锂氧化物,但它也可以是锂碳酸盐或锂矿物,它取代了对萤石(氟化钙)的需要。
在空气处理过程中,锂盐的应用也十分广泛,涉及冷却和干燥等环节。例如,溴化锂在工业空气冷却系统中被用作冷却剂。此外,氯化锂和溴化锂组合后也可用作风干干燥系统。氢氧化锂则是一种有效的二氧化碳清除剂,常见于太空船或潜艇等特定场景。
铝的前端生产中,锂的使用量很少。在进行金属铝制备时,为了降低氧化铝(氧化铝的熔点为2072度)的熔点,通常需要引入一种助熔剂。一种常见的助熔剂是低温石(氟化钠)。然而,也可以使用锂盐,如碳酸锂或氯化锂。这些锂盐在与加入的冰晶石反应后会形成氟化锂。采用锂盐的优点在于:可以进一步降低工艺温度,同时提高熔体的电传导性能,从而减少电解反应过程中的过电位需求。
药剂学:在这里,主要使用碳酸锂作为双相情感障碍治疗的情绪稳定剂,同时锂也用于皮肤软膏、减肥药物、艾滋病药物甚至癌症治疗中。
最后一个例子是锂聚合物的合成。锂盐常作为催化剂,例如苯基锂催化剂用于合成橡胶,如苯乙烯丁二烯弹性体、聚丁二烯橡胶,甚至用于生产管状塑料或丙烯酸漆。此外锂还用于生产铌酸锂(LiNbO3)和钽矿(电容器的重要原料)。ITER是一个大的核聚变实验,其中使用了锂6同位素来制造氚。此外,在水泥中加入锂盐可以加速其硬化过程。醋酸锂可用于纺织面料。
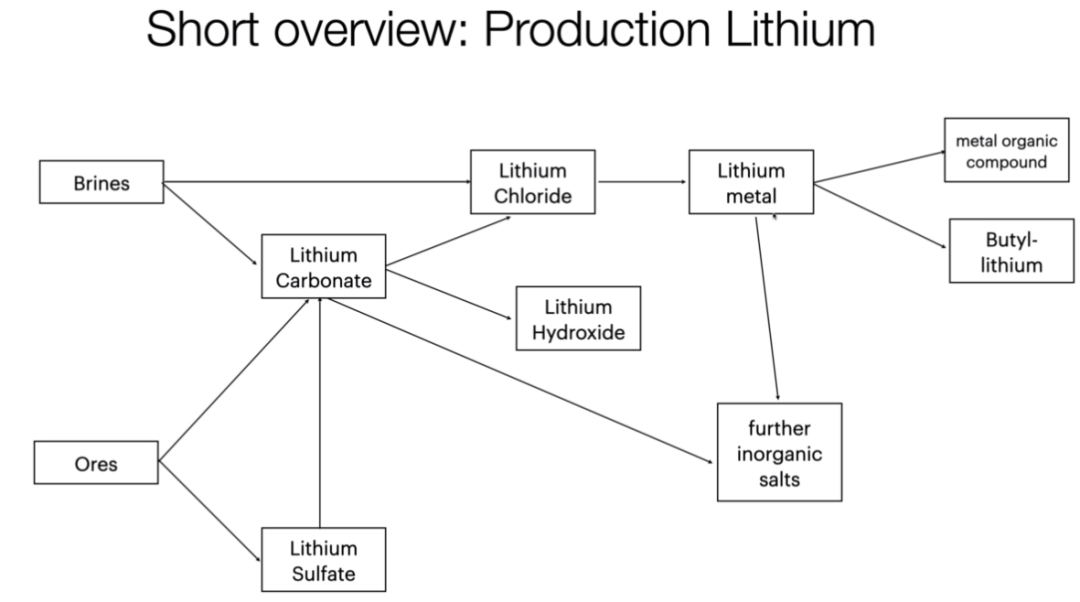
锂矿床的提炼过程涉及从岩石中剥离出特定的锂矿石,这些矿石或卤水构成了初级产品,进一步从中提取并浓缩锂矿物。通常,卤水中的锂以碳酸锂的形式存在。随后,通过对矿物浓缩物实施不同处理,可获得氢氧化锂、氯化锂、溴化锂、硬脂酸锂等系列次级产品。这些产品在玻璃、陶瓷、钢铸造、铝生产、碳捕集、锂离子电池、制药、润滑剂、空调、合金制造、催化剂等众多行业中有着广泛应用,彰显了锂在工业领域的多元用途。
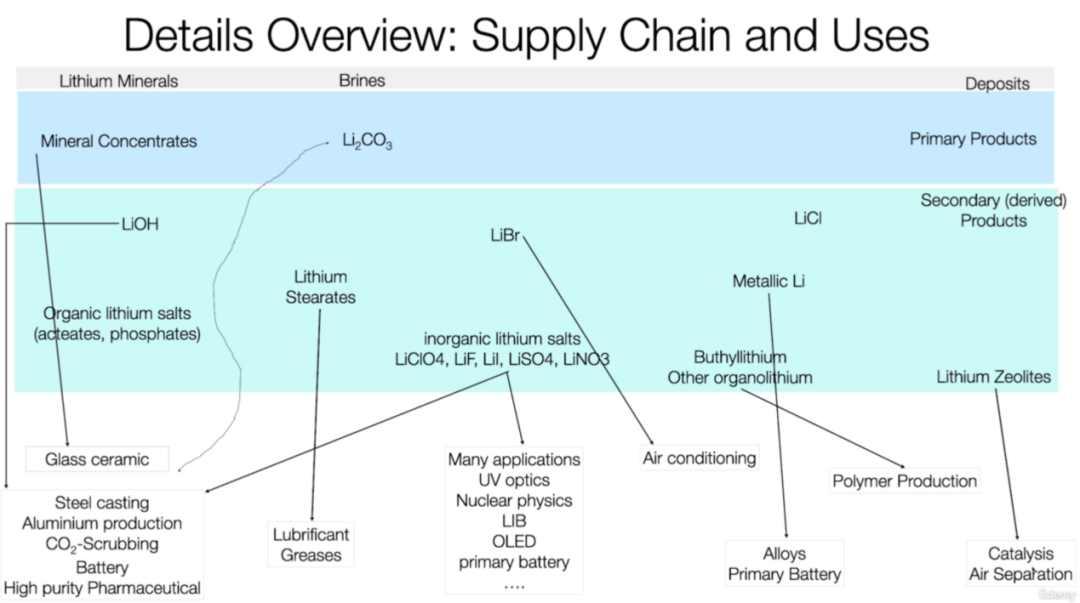
此外,次级产品如硬脂酸锂和各类无机锂盐在润滑剂、电池、制药、烟花、紫外线光学等领域有着广泛应用。溴化锂主要应用于空调,金属锂则用于合金制造和初级电池。有机锂化合物,如丁基锂,主要作为聚合物生产的催化剂。部分特殊化学物质,如沸石,也在催化和空气分离等领域发挥作用。这表明锂在工业领域具有广泛且多样的应用。

观察2000年、2001年、2002年、2003年、2004年,电池产业并未显现出显著的重要性。然而,这一状况很快发生了改变,尤其在2010年以后。我们发现,越来越多的锂资源被应用于可充电电池领域,占比逐年上升,目前已超过一半。因此,锂资源的运用在很大程度上改变了原有稳定态势,与陶瓷、玻璃、润滑脂等产品的应用相比,电池产业的重要性日益凸显。
锂元素主要蕴含于硅酸盐之中,普遍存在于伟晶岩和花岗岩类岩石中。其存在的原因源于锂离子具有较小的离子半径,它是周期表中的第三元素,因此体积较小。锂无法替代较大的碱金属离子,如钠、钾和铯等,这些离子在岩石形成矿物中普遍存在。然而,锂能够替代铁、铝或镁离子。这是因为我们在常见的岩石形成矿物中难以找到锂,或在部分矿物中仅能发现其存在,如富含镁的黑云母等。事实上,锂在岩浆中得以富集。熟悉这一过程的人都知道,这便是Boven-Serie现象。当岩浆冷却结晶时,随着温度下降,各类岩石和矿石家族相继结晶而成。这一现象被称为差异结晶。由于锂无法适应岩石形成矿物,它会在岩浆冷却过程中逐渐富集。因此,锂元素最终会出现在典型的“酸性”岩石中,如花岗岩、流纹岩等。
锂之所以能够取代铁、铝或镁离子,主要得益于其独特的离子半径和电性质。作为第三周期元素,锂具有较小的离子半径和较高的电荷密度。在晶体结构中,矿物中的各元素均占据特定位置,形成稳定的结构。锂的小离子半径使其能够替代较大离子,如铁、铝或镁。尽管这种替代通常会导致结构变化,但鉴于锂较高的电荷密度,仍能在晶格中找到恰当位置,维持整体稳定性。
总之,锂的替代性相对有限,主要发生在特定类型矿物和结构中。这种替代性现象在地球化学和矿石形成过程中具有重要意义,尤其对于地质过程中的含锂矿床形成。
锂最终出现在典型的“酸性”岩石(如花岗岩、流纹岩)中,与其在岩浆演化过程中的化学性质有关。在地球科学中,岩浆演化指的是岩浆(熔融状态的岩石物质)从地下深处上升至地表并冷却结晶的过程。
锂通常在岩浆演化的早期阶段就会被富集。当岩浆冷却结晶时,不同的矿物相会逐渐结晶并沉淀出来,这被称为差异结晶。由于锂的离子半径和电性质使其难以被一些常见的岩石矿物所容纳,因此锂倾向于在岩浆中富集,而不会随着其他矿物的结晶而结合成固体。
在这个过程中,形成的岩石通常是酸性的,富含石英、长石等矿物,从而形成花岗岩或流纹岩。这些岩石类型中锂的浓度相对较高,因为锂无法像其他岩石矿物中的一些离子那样被牢固地固定在晶格中。因此,锂在这些酸性岩石中被经济上富集,形成了可开采的锂矿床。
1. 玻利维亚:拥有约两千一百万吨的锂储量,是世界上最大的锂储量国之一,主要位于南美洲的一个三角地带。
2.阿根廷:拥有约一千七百万吨的锂储量,主要分布在Santos和Sissala矿床中。2019年,阿根廷产出约6400吨锂金属。
3.智利:拥有约九百万吨的锂储量,是世界上第三大锂储量国。智利在锂开采方面取得了良好的发展,是全球第二大锂生产国,年产量约为18000吨。
4.美国:拥有大约六百八十万吨的锂储量,是世界第四大锂储量国。然而,美国的锂生产量相对较低,主要集中在内华达州的一个项目。
5.澳大利亚:拥有约六百三十万吨的锂储量,是全球最大的锂生产国。2019年,澳大利亚的年产量约为42000吨,主要来自硬岩和莫来矿的开采。
6.中国:拥有约四百五十万吨的锂储量,是世界第六大锂储量国。中国是全球第二大锂生产国,年产量为7500吨。
7.此外,葡萄牙、津巴布韦和阿富汗等国家也拥有一定数量的锂储量。
根据全球矿床分布特征可以发现,盐湖卤水型锂矿床形成于多风、少雨、干燥的气候环境下的封闭汇水盆地内,周围新生代火山活动频繁,断层发育,赋锂围岩、岩浆热液活动和火山喷出物等提供了丰富的物质来源,在长期的地质作用和气候条件的影响下,汇聚蒸发形成矿床。
全球已发现的所有盐湖卤水型锂矿床均分布在新生代干燥盆地,例如,南美洲安第斯高原赋锂盐湖群位于安第斯山脉的高寒气候区,安第斯山脉构成雨水隔离带,使得盆地内年蒸发量是年降水量的17倍(表1);青藏高原的隆升阻挡了来自印度洋的暖湿气流,促使高原气候向干寒方向发展,在高原的中部、西部和北部形成了众多的盐湖,其中富锂盐湖80多个(Licl≥300ppm);美国西南部赋锂盐湖群位于太平洋海岸山脉与落基山脉之间,位置深居内陆、海洋水汽难以进入,形成干燥少雨的内陆型气候。锂在整个化学风化过程中都是可溶解的,在封闭的盆地中,尤其是高蒸发区,锂大部分残留在卤水中,并随着蒸发风化进行富集成矿。此外,成矿区周围一般高山环绕,例如,阿塔卡玛盐湖所处的智利北部阿塔卡玛盆地,东西两侧分别分布有安第斯山脉及太平洋海岸山脉,山区与盆地之间的高程差达到了2000m以上。数千米的高程差形成了水文气候的差动效应,山脉高峻能阻隔季风,高山迎风区雨量较多,而盆地内背风区因雨影效应极度干旱。同时,来自山区的季节性水流汇聚入盆地,在盆地中进行强烈的蒸发,卤水中的溶质锂在封闭系统中进行自然富集浓缩,数万年以上的循环往复,足以成矿。
高原地区的含锂原岩是盐湖卤水型锂矿床成矿物质的重要来源。高原地区的山系中广泛分布着各个时期的花岗岩、花岗斑岩、长英质凝灰岩、含锂伟晶岩和黏土岩等,在岩石的风化过程中锂被淋滤溶解,随着河流汇聚入成矿盆地。例如,柴达木盆地周边基岩易溶盐含量明显高于其他地区,且成分分布与察尔汗盐湖含量分布情况相吻合。同时,周边火山系统及地下岩浆体所产生的地热活动带出的成矿物质,随着河流和地下水系统携带进入盆地,构成了盐湖卤水型锂矿床的又一主要物质来源。例如,阿塔卡玛盐湖近1/10的锂来自于EiTatio地区的间歇泉,安第斯高原地区分布有众多的新生代火山和地下热泉,地下热水将近期火山活动形成的地热流体或岩石中的锂、硼等成矿元素淋滤浸出,沿断层上涌形成间歇泉,该间歇泉从盆地北部汇入里约圣佩德罗河,最终流入盐湖中,河水中的Li浓度达到了26~47ppm;柴达木盆地内相距较近的发育了一里坪盐湖、东西台吉乃尔盐湖三个大中型赋锂盐湖,其主要成矿物质来源于那棱格勒河,该河沿昆南断裂分布,断裂带两侧存在一系列新生代火山活动,河水溶解了与火山及断裂活动有关的温泉热水中的成矿物质,使得河水中的Li浓度较盆地中其他河流高出了50~100倍;相关研究证明,银峰盐湖锂的主要来源为沿银峰断裂上涌而来的热泉流,盐湖内深25.5m处的卤水温度高达44℃形成了有力的佐证。
另一种重要的锂来源是发生在盆地地质史较早期的湖泊沉积床。例如,柴达木盆地经历了上新世末和中更新世末的两次大规模构造运动,使得古近纪开始沉积形成的柴达木古湖肢解成几个次级盆地,从而形成了察尔汗盐湖,使其继承了古湖的盐类物质;扎布耶盐湖在晚更新统也经历了“泛湖时期”,汇水范围广阔,聚集了大量B、Li成矿物质,同时在盆地内发现的中新世富B、Li火山沉积,也是其重要的一个物质来源。此外,大多地区的新生代地层中及高矿化度的油田水(级深部地层水)中均普遍含有锂,也构成了盐湖卤水型锂矿床的物质来源。例如,柴达木盆地内广泛分布油田水,在察尔汗盐湖形成早期,构造活动强烈,油田水通过断层流入盐湖,是成矿物质的重要补给来源之一。就卤水含量特征而言,锂有很高的溶解度,不像钠、钾、钙在蒸发浓缩时会形成蒸发盐矿物,取而代之的是,锂在浅层(一般不超过50m)地下存在于蒸发剩余的卤水中,有经济价值的卤水含锂浓度通常为200~4000mg/l的范围。盐壳中锂含量与深度、密度、孔隙度有关,深层锂含量与蒸发岩、沉积岩排列有关。水岩反应也被认为增加了卤水组分,例如,扎布耶盐湖地区的地层中Li、B等成矿元素相对其他矿区含量较低,但经历了长期风化淋滤及浸泡等水岩交互作用,成矿元素较容易被浸出,并随河流不断向湖中迁移,形成了盐湖成矿物质的来源之一。就卤水分布特征而言,与断层作用直接相关。例如,阿塔卡玛盆地中心的形成于沉积时期的深大断裂(沿NNW向展布)导致东西两侧沉积厚度相差240m,从而导致盆地东西卤水分布深度不同;在克莱顿河谷的卤水都沿活动的盆地内断层分布。似乎所有的锂矿盆地都经历过断层活动,例如,扎布耶盐湖区发育有大量的断陷盆地和复杂的褶皱和断裂;察尔汗盐湖所在的柴达木盆地地质构造活跃,尤其是盆地西部地区新近纪、古近纪地层中一系列的构造裂隙、孔隙为地下水的储存提供了巨大的空间;而相比在克拉通地区,较浅、较接近的盆地,如撒哈拉沙漠缺少断层活动控制,也就没有卤水型锂矿的前景可言。盆地本身只有很薄的孔隙可以供沉积累积,但断层引起的下沉创造了更大的可容空间,较厚的盆地充填沉积提供了足够体积的蓄水层储存可利用的卤水资源。
此外,断层还是地下热流上升的良好通道,为盐湖提供了重要的成矿物质的补给。同时,新生代构造活动活跃是盐湖卤水型锂矿床又一个重要的成矿特征。例如:南美洲赋锂盐湖群分布在安第斯山脉的普纳高原上,形成于白垩纪末至古近纪,目前地壳活动仍然比较剧烈;青藏高原赋锂盐湖群是位于喜马拉雅山造山带挤压断层上盘,在封闭盆地中存在大量深部岩浆热液活动;美国西南部赋锂盐湖群处于一个外延的半地堑系统中,在中生代—新生代造山活动旋回期间形成,目前存在多处活火山。
根据上述盐湖卤水型锂矿床的不同构造特征,可将赋锂盐湖进一步划分为:后弧挤压盆地大陆型盐湖、后弧扩张克拉通盆地盐湖以及前陆和后陆山问槽地和盆地区的盐湖。
1)有断层活动的封闭盆地是形成盐湖卤水型锂矿床的必要条件。盆地的封闭性是决定非海成盆地能否堆积含锂卤水的一个重要因素,而封闭盆地是构造作用的产物,断层活动导致地层下沉,为成矿物质的沉降提供了必要空间,同时,沿断层运移上来的富锂热液提供了必要且丰富的成矿物质。
2)干旱的气候也是形成盐湖卤水型锂矿床必不可少的成矿条件。封闭盆地的存在依靠于区域长时间的蒸发量大于降水量,如果盆地的降水率长期增长较快,最终含锂卤水将超过分水岭并排出盆地。这种气候条件使湖泊中含少量盐分的淡水不断浓缩,通常赋锂盆地的年蒸发量是降雨量的10~200倍。
3)由于赋锂的封闭盆地构造上需要经历沉降,从年轻的火山或热泉而来的热流和富锂火山灰是成矿物质的重要来源,所以,新生代地质活动较为活跃也是盐湖卤水型锂矿床的一个重要找矿标志。





α-锂辉石在经过粉碎后,可在950~1100℃的条件下焙烧转变为β-锂辉石。接下来,在2.250~300℃的温度下,将其与硫酸混合进行焙烧。随后,进行水浸处理。在浸出液中,加入石灰粉以中和过量的硫酸,并调节pH值至近中性(6.0~6.5),以去除浸液中的Fe和Al。接着,加入石灰乳以去除大部分Mg。最后,通过碳酸钠在pH=11~13的条件下,深度去除Mg和Ca。经过蒸发浓缩,可得到含锂约20%的硫酸锂净化液。碳酸钠可用于沉淀碳酸锂,其回收率可达90%左右。
然而,该工艺中硫酸的消耗量较大,通常为理论用量的1.5倍。酸化焙烧过程易产生含硫废气。在锂浸出后,会产生大量的硅铝废渣。同时,在余酸中和过程中,还会产生大量的硫酸钙及其他废渣。每生产1 t碳酸锂,将排出8~10 t锂渣。这些废渣量大,难以利用,储存占用大面积土地,造成环境污染严重。因此,锂渣的利用已成为清洁生产的重要环节,引起了广泛关注。
碱法提取锂辉石工艺主要包括石灰石法、碳酸钠焙烧碱法和纯碱压煮法三种。
石灰石焙烧法的选矿工艺流程大致如下:
1. 将锂辉石与石灰石按1∶(3.05~3.15)的质量比加入水中制成料浆;
2. 在800~900℃的条件下进行焙烧;
3.进行水浸处理,沉降分离以去除钙、铝、硅等杂质;
4. 将除杂后的氢氧化锂溶液进行浓缩,通入二氧化碳或添加碳酸钠沉淀碳酸锂。该工艺的锂总收率为70%~80%,但在浸出过程中需要保证熟料中有过量的氧化钙,否则难溶铝酸锂会与氢氧化钙反应生成氢氧化锂。然而,该工艺存在浸液浓度低、蒸发能耗大、出渣量大等问题,生产1吨锂盐会排出约20吨碱性锂渣,经济效益较差,目前已基本被淘汰。
碳酸钠焙烧碱法的选矿工艺流程大致如下:
1. 将碳酸钠与β-锂辉石混合后在800℃下焙烧;
2.采用盐酸进行浸出处理;
3. 用氢氧化钠沉淀去除铝杂质;
4. 用碳酸钠沉淀碳酸锂。在酸浸过程中,硅形成的硅酸可以作为制备硅产品的原料,铝经过氢氧化钠沉淀得到的铝沉淀物纯度高,具有进一步利用的价值,废渣排放量大大减少。然而,该工艺的缺点是碱和酸的耗量大,中和过程中会产生大量的氯化钠,导致工艺运行成本较高,尚未见到工业化应用。
纯碱压煮法的选矿工艺流程大致如下:
1. 将β-锂辉石与碳酸钠溶液(约105g·L-1)在225℃下进行压煮反应,使锂形成碳酸锂结晶;
2.向浆料中通入二氧化碳,使碳酸锂形成溶解度更大的碳酸氢锂;
3.加热滤液以析出碳酸锂结晶。锂的提取率可达96%以上。
针对硫酸工艺导致的严重污染、硅铝废渣大量堆积难以利用,以及碱法工艺中碱耗大、成本高等问题,本研究探讨了盐焙烧工艺。在诸多焙烧方法中,硫酸盐焙烧法的研究较为深入。其主要工艺步骤如下:
1.锂辉石精矿与K2SO4(或CaSO4或两者混合物)在920~1100℃下进行焙烧;
2.进行水浸处理;
3. 将浸液中加入NaOH,用以沉淀Fe、Al等杂质;
4.蒸发浓缩处理;
5. 通过碳酸钠沉淀碳酸锂。
高温氯化提取锂的工艺是以Cl2为氯化剂对β-锂辉石进行氯化焙烧提取LiCl。在Cl2流速为100 ml·min-1,1100℃下焙烧15 min,Li的转化率达到90%以上。由于反应在流动的系统中进行,生成的挥发性LiCl被氯气气流带离,促使反应进行完全。
此工艺简单,仅采用单一的氯化试剂,产生的硅铝渣量少且易利用。但LiCl收集困难,炉气腐蚀性强,工业实施难度大。
盐湖提锂常用工艺有太阳池法、吸附法、萃取法、膜法、电化学法等,各工艺优缺点及商业化项目见下表。
主要卤水提锂工艺商业化现状及优缺点对比
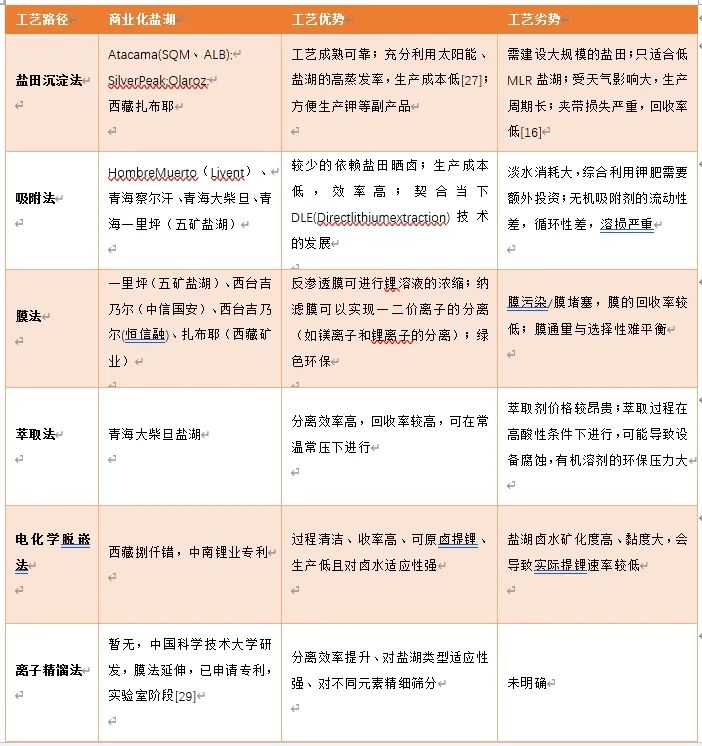
MLR(镁锂比)在工业提锂中起着决定性的作用,基础的盐田沉淀法仅适用于低MLR盐湖,而实际上世界大多数盐湖的MLR均高于8甚至达到数千,为高MLR盐湖,下表总结了世界主要盐湖的MLR。针对世界主要在产盐湖多为高MLR盐湖这一特征,当前盐湖提锂应解决的核心问题是“镁锂分离”,二者在元素周期表中呈特殊对角线关系,性质相近因此分离的难度大。

膜分离技术已被证实是实现分子和离子高效分离的重要手段之一。在压力、浓度、热能和电位差等外部驱动力作用下,膜的选择性渗透率特性使得进料溶液中的各个组分能够有选择性地透过膜。膜分离技术具有能耗低、操作简单、环保、可连续等独特优势,可同时实现目标物质的分离、纯化和浓缩。膜材料根据孔径范围的分类见下表:

纳滤膜以其独特的道南效应在镁锂分离领域展现出巨大的潜力。这种带正电荷的膜表面能够形成高表面势垒,有效地阻止阳离子靠近,使得纳滤膜在处理二价镁离子和一价锂离子的过程中展现出出色的选择性。同时,基于库仑定律,荷正电的纳滤膜对二价Mg2+的排斥作用强于对一价Li+的排斥作用。一价锂离子的排斥力较小,因此更容易通过膜。而国内也有着这么一家具有自主知识产权的分离膜工业龙头企业,它正是江苏久吾高科技股份有限公司专注从事陶瓷膜、有机膜等膜材料及膜分离技术的研发与应用,是江苏省首批认定的国家高新技术企业、国家火炬计划高新技术企业、国家“专精特新”小巨人企业。公司于2017年3月在深交所A股创业板上市。公司是首批认定的国家级高新技术企业、国家专精特新“小巨人”企业、国家制造业单项冠军、中国膜行业陶瓷膜领域龙头企业,先后获得四次国家科学技术进步奖、一次国家技术发明奖和中国专利优秀奖。
成立二十多年来,公司建成了从新材料研制、技术开发、工艺设计、成套设备制造到提供整体解决方案、项目运营等完整的业务产业链。公司求索不止,在陶瓷膜、有机膜、吸附剂等新材料制造领域不断取得突破。以此为基础,为新能源服务、工业流体分离、水处理与资源化利用、工业废石膏资源化利用等四大领域提供整体解决方案。特别在盐湖提锂、电池正极材料、废盐综合治理、生物燃料乙醇、氯碱化工、生物制品等多个细分领域实现了突破性的创新应用。目前公司产品远销全球四十多个国家和地区,得到了国内外客户的广泛认可。作为中国民族工业的一面旗帜,公司始终以市场为导向,引领创新发展。坚持新材料与整体解决方案双轮驱动,为客户创造价值,为人类守护未来。

如图所示是使用传统方法制备锂金属阳极的工艺原理示意图。常规锂金属的产生过程主要包括从含水层中提取含大量溶解盐的盐水,然后泵入浅层蒸发太阳能池,蒸发过程使盐水富集,直到产生氯化锂,然后与碳酸钠反应生成金属锂最常见的前体Li2CO3。然后将Li2CO3与HCl反应得到LiCl,再将LiCl进一步转化成金属锂。图展示了电解法获得锂金属的原理示意图。一个典型的电解池由石墨阳极和低碳钢阴极浸没在熔融的LiCl-KCl电解质中组成。新形成的锂金属润湿钢阴极表面,形成熔融金属池。液态锂取出后并冷却至约300°C。获得的锂金属锭将其挤压形成薄膜。
废旧锂电池的回收方法主要有物理法、化学法和生物法三大类。与其他方法相比,湿法冶金因其能耗低、回收效率高及产品纯度高等优点被认为是一种较理想的回收方法。
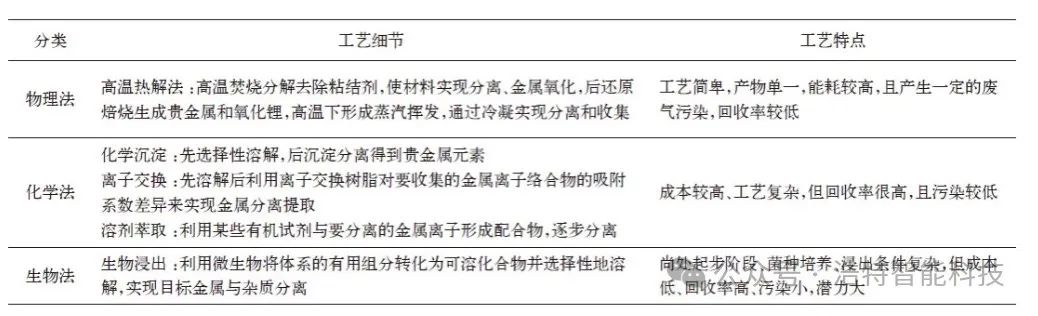
物理法
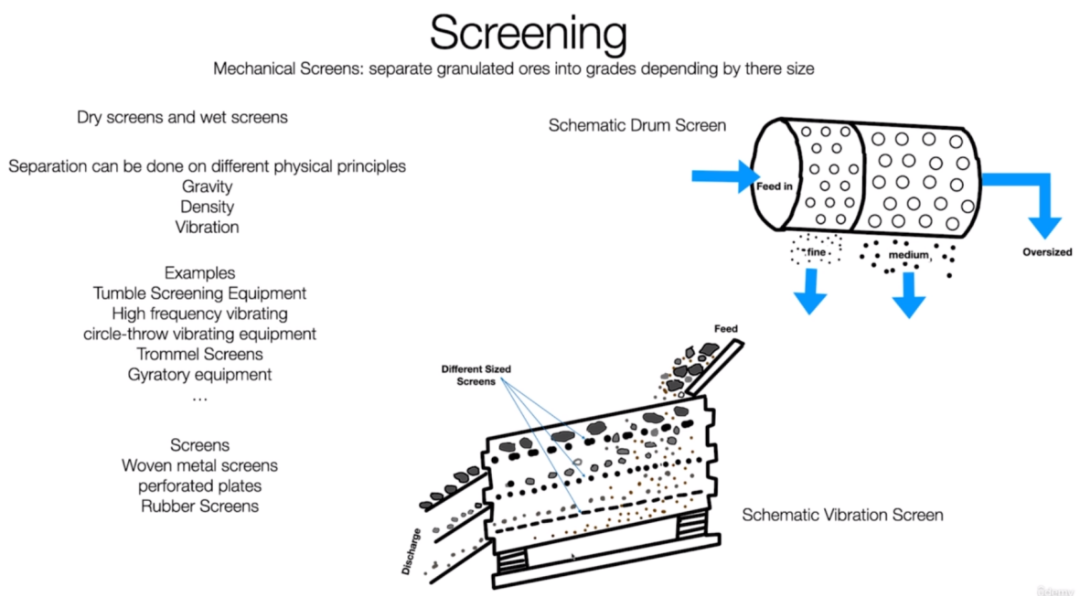
物理法利用物理化学反应过程对锂离子电池进行处理。常见的物化处理方法主要是破碎浮选法和机械研磨法。
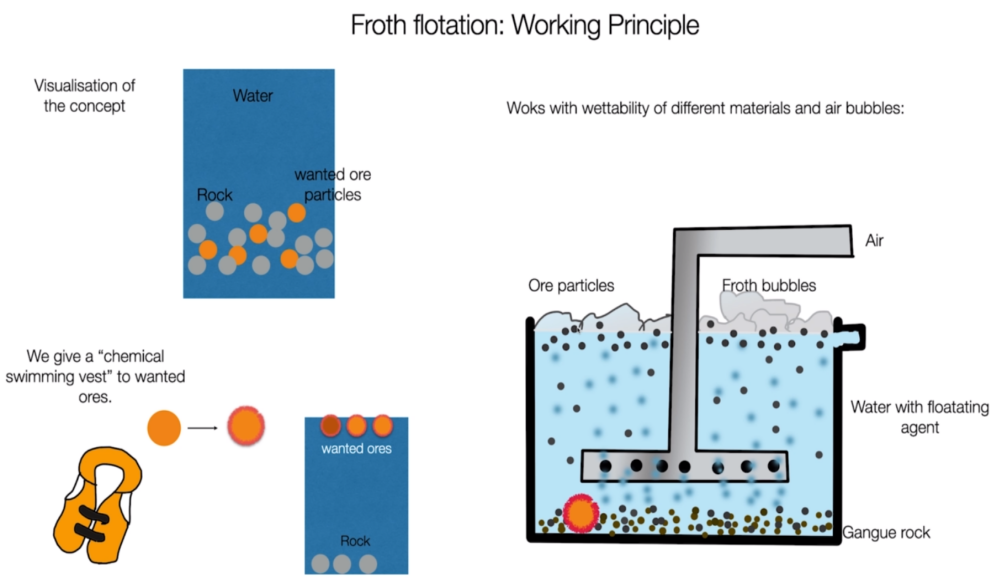
1) 破碎浮选法
破碎浮选法是利用物质表面物理化学性质的差异进行分选的一种方法,即首先对完整的废锂离子电池进行破碎、分选后,将获得的电极材料粉末进行热处理去除有机粘结剂,最后根据电极材料粉末中钴酸锂和石墨表面的亲水性差异进行浮选分离,从而回收钴锂化合物粉体。破碎浮选法工艺简单,可使钴酸锂与碳素材料得到有效分离,且锂、钴的回收率较高。但是由于各种物质全部被破碎混合,对后续铜箔、铝箔及金属壳碎片的分离回收造成了困难; 且因为破碎易使电解质LiPF6与H2O 反应产生HF 等挥发性气体造成环境污染,需要注意破碎方法。
2) 机械研磨法
机械研磨法是利用机械研磨产生的热能促使电极材料与磨料发生反应,从而使电极材料中原本黏结在集流体上的锂化合物转化为盐类的一种方法。不同类型的研磨助剂材料的回收率有所区别,较高的回收率可以做到:Co 回收率98%,Li 回收率99%。机械研磨法也是一种有效的回收废旧锂离子电池中钴和锂的方法,其工艺较简单,但对仪器要求较高,且易造成钴的损失及铝箔回收困难。
化学法
化学法是利用化学反应过程对锂离子电池进行处理的方法,一般分为火法冶金和湿法冶金2 种方法。
1) 火法冶金
火法冶金,又称焚烧法或干法冶金,是通过高温焚烧去除电极材料中的有机粘结剂,同时使其中的金属及其化合物发生氧化还原反应,以冷凝的形式回收低沸点的金属及其化合物,对炉渣中的金属采用筛分、热解、磁选或化学方法等进行回收。火法冶金对原料的组分要求不高,适合大规模处理较复杂的电池,但燃烧必定会产生部分废气污染环境,且高温处理对设备的要求也较高,同时还需要增加净化回收设备等,处理成本较高。
2) 湿法冶金
湿法冶金是用合适的化学试剂选择性溶解废旧锂离子电池中的正极材料,并分离浸出液中的金属元素的一种方法。湿法冶金工艺比较适合回收化学组成相对单一的废旧锂电池,可以单独使用,也可以联合高温冶金一起使用,对设备要求不高,处理成本较低,是一种很成熟的处理方法,适合中小规模废旧锂离子电池的回收。
生物法
生物冶金法目前也在研究进行中,其利用微生物菌类的代谢过程来实现对钴、锂等金属元素的选择性浸出。生物法能源消耗低,成本低,且微生物可以重复利用,污染很小; 但培养微生物菌类要求条件苛刻,培养时间长,浸出效率低,工艺有待进一步改进。
磷酸铁锂回收偏冷门
在多种动力锂电池中,只有磷酸铁锂电池正极材料不含贵金属,而是主要由铝、锂、铁、磷和碳元素组成。正因如此,企业对磷酸铁锂的回收分解并不热心。对磷酸铁锂电池回收,有针对性的研究也比较少。
磷酸铁锂的一般处理方式是电池整体经机械粉碎后,利用极性有机溶剂NMP或强碱溶解分离其中的铝,剩余的材料即为LiFePO4 和碳粉的混合物。向该混合物中引入Li、Fe、P 以调整此三种元素在材料中的摩尔比,再经球磨、惰性气氛下高温煅烧后可重新合成LiFePO4材料,但与首次合成的磷酸铁锂电池正极材料相比,该材料的电容量、充放电性能均有所下降。将失效磷酸铁锂电池正极材料氧化分解,回收锂、铁、磷、碳并重新利用才是治标治本的回收路径。
研究虽少,总归还是有人在做。比如祝宏帅等开发了一种方法,用磷酸体系浸取失效磷酸铁锂电池正极材料,以高效率、低成本、零废料排放的方法实现更好的锂、铁分离效果,综合回收锂、铁、磷、碳。
通过对国内外锂离子电池回收工艺的研究可以看出,使用物理化学法回收锂离子电池的回收率较低; 化学法研究普遍,应用范围广,相对比较可行; 生物法虽环保,但所需时间太长,有待进一步研究。针对化学法的众多研究表明: 通过单一火法冶金不及通过湿法冶金获得的再生材料的电化学性能好,但通过单一湿法冶金回收需要大量的试剂,不适合大规模工业化处理。
比较而言,湿法冶金是当前提取方法中综合性能比较好的一类方法,酸浸出是其中最重要的环节。其主要目的是将预处理后的活性物质中的目标金属转移到浸出液中,便于后续的分离回收过程。传统的无机强酸(HCl、HNO3和H2SO4)已经被广泛运用于浸出过程。然而,在浸出过程中会伴随产生有毒气体如Cl2、SO3以及Nx等对环境造成危害。因此,近年来研究者们开始关注有机酸(柠檬酸、草酸、抗坏血酸等)在浸出过程中的作用。而与传统的无机酸相比,有机酸浸出在满足高效率的同时能够减少对环境的二次污染。
典型的湿法提取主要步骤:预处理→酸液浸出→浸出液除杂→分离萃取→元素沉淀。
预处理基本步骤
将废旧锂电池放入食盐水中放电,除去电池的外包装,去除金属钢壳得到里面的电芯。电芯由负极、正极、隔膜和电解液组成。负极附着在铜箔表面,正极附着在铝箔表面,隔膜为有机聚合物;电解液附着在正、负极的表面,为LiPF6 的有机碳酸酯溶液。
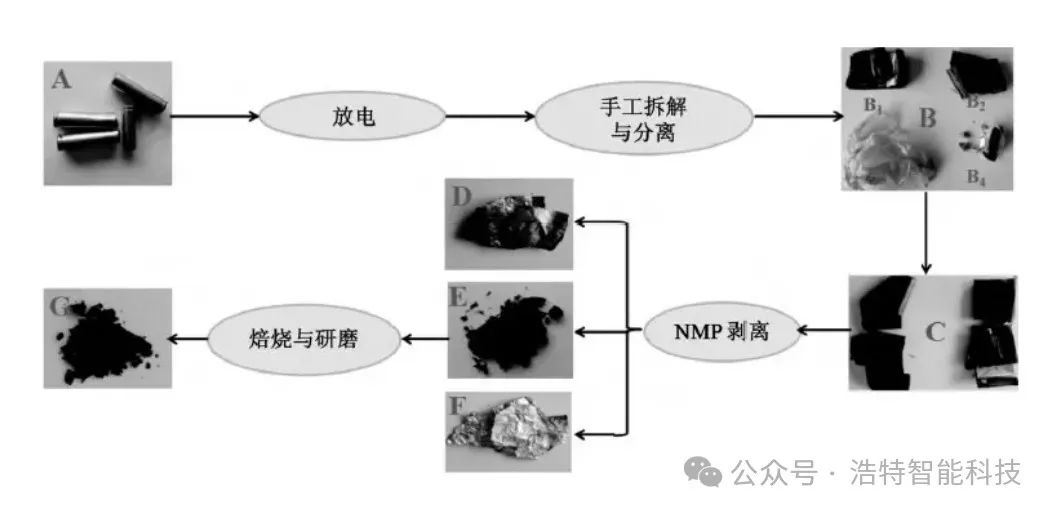
典型的浸出萃取操作:从一个完整电芯,经过预处理后,成为粉末状待处理原料。不同工艺,后续处理手段差别较大。典型的湿法提取步骤如下:
1)在硫酸溶液中加入LiCoO2电极粉末,保持特定固液比,机械搅拌;
2)超声波浸出60min 后,滤去残渣,测定浸出液中各金属的浓度;
3)然后加入碳酸氢铵溶液调节浸出液的PH值为,静置过滤后,加入少量的Na2S 溶液除铜;
4)采用P507-磺化煤油体系萃取钴,用H2SO4 反萃,从而得到高纯度的硫酸钴溶液;
5)之后将NaOH 溶液和富钴溶液加热至沸腾,往富钴溶液中加入碱溶液,直至钴溶液中产生大量的蓝色沉淀为止;
6)将烧杯口封起来,静置5min 后,蓝色沉淀完全转变为粉红色沉淀氢氧化钠沉钴;
7)多次洗涤,加入乙醇作为分散剂陈化后,过滤,将滤饼于105℃烘干后得到的物质放入马弗炉中煅烧,得到黑色粉末状四氧化三钴。
作者简介:
中国矿业大学(北京)矿业工程硕士(在读)
主要研究方向为盐湖提锂相关的纳滤膜的研究。本科毕业于贵州大学,专业为矿物加工工程。本科期间获得过挑战杯科技作品竞赛省级三等奖,挑战杯创业计划竞赛校级一等奖,校奖学金等。有松河选煤厂、瓮福磷矿厂等实习经验。研究生阶段,参与过汉源锂矿厂智能化改造实习,目前正参与节能减排大赛(基于AI算法的磨矿功率优化)、挑战杯(ChatGPT+预测性维护)等多项赛事。
X
欢迎来到浩沃特!


























